Tutkimus
Tutkimus
Meneillään olevia tutkimuksia
Meneillään olevia tutkimuksia
KML- tutkimukset
KML- tutkimukset
Käynnissä olevista KML- tutkimuksista tarkemmin KML- osion alasivulla.
HRUHLAB2
HRUHLAB2
Tutkimuksen nimi: "Veritautien molekylaarinen patogeneesi, altistavat tekijät ja yksilöllistetty hoito"
| Tutkimuksen vastuuhenkilöt | Prof. Kimmo Porkka, prof. Satu Mustjoki, LT Mika Kontro |
| Tutkimuksen lyhenne | HRUHLAB2 |
| Tutkimuksen suorituspaikka | Hematologinen tutkimusyksikkö (HruH), ja FIMM, Helsigin yliopisto; Sairaanhoitopiirit |
| Tutkimuksen tyyppi | Ei-kajoava laboratoriotutkimus |
| Tutkimuksen aloituspäivä | 01.02.2012 |
| Tutkimuksen status | Käynnissä, rekrytoi potilaita |
| Tutkimuspopulaatiot | Kaikki veritauteja sairastavat potilaat |
Tutkimuksen tausta, tavoitteet ja toteutus
Vaikka usean pahanlaatuisen veritaudin hoidossa onkin viime vuosina saavutettu merkittäviä edistysaskeleita, on mm. akuuttien leukemioiden hoito pysynyt valtaosin ennallaan. Pahanlaatuiset veritaudit ovat sangen monimuotoinen tautiryhmä, eikä taudin mekanismien löytämisessä ja hoidossa ole toistaiseksi saavutettu edistysaskeleita. Suurimman haasteen nykyhoidoille asettavat uusiutuneet tai hoidolle vastaamattomat leukemiat. Yhä edelleen yli puolet potilaista menehtyy hoidon haittavaikutuksiin tai hoidolle reagoimattomaan leukemiaan.
Valtaosa kliinisessä käytössä olevista tutkimusmenetelmistä on vielä riittämättömiä molekylaaristen hoitokohteiden tunnistukseen ja kohdennetun hoidon valintaan. Oikean kohdennetun hoidon löytäminen saattaa kuitenkin parantaa ennustetta - suotuisana esimerkkinä on ollut tyrosiinikinaasiestäjien käyttöönotto Ph-positiivisessa akuutissa lymfaattisessa leukemiassa ja kroonisessa myelooisessa leukemiassa.
Pahalaatuisten verisairauksien hoidon tulosten parantamiseksi tarvitaan uudenlaisia menetelmiä. Uskomme, että selvittämällä syöpäsolujen geneettisten poikkeavuuksien sekä geenien ilmentymän ja signaalivälityksen muutoksia voimme löytää aiemmin tuntemattomia ennusteellisia ja hoidollisia tekijöitä. Yhdistämällä näitä tuloksia ex vivo –lääkeaine-herkkyyksien tuloksiin, voidaan puolestaan löytää uusia hoidollisia kohteita ja lääkevastetta ennustavia tekijöitä. Lisäksi tutkimme eri hoitomuotojen vaikutuksia syöpäsoluihin sekä myös elimistön normaaleihin soluihin ja pyrimme löytämään tekijöitä, jotka saattavat olla eri hoitomuotojen haittavaikutusten takana. Selvitämme myös perinnöllistä alttiutta sairastua pahanlaatuisiin verisairauksiin. Tutkimus suoritetaan yhteistyössä Suomen Molekyylilääketieteen instituutin (FIMM) kanssa.
Näytteenotto-ohjeet
Näytteenotto-ohjeet
Tutkimuksen tausta
Veritauteja (mm. akuutit leukemiat, myelooma) sairastavilta potilailta kerätään näytteitä ”Veritautien molekylaarinen patogeneesi, altistavat tekijät ja yksilöllistetty hoito”. Tutkimustiedote löytyy hematology.fi sivuilta (HRUHLAB2).
Tutkimuksessa potilailta kerätyistä näytteistä (pääosin luuydin- tai verinäytteistä) tehdään eksomisekvensointi, RNA-sekvensointi, sekä ex vivo lääkeherkkyystutkimus (drug sensitivity and resistance testing, DSRT). Lääkeherkkyystutkimuksessa syöpäsolut altistetaan laboratorio-olosuhteissa useille lääkeaineille.
Yhdistämällä geneettinen tieto lääkeherkkyystuloksiin toivomme löytävämme uusia kohteita veritautien lääkekehitykselle sekä pääsemään askel lähemmäksi potilaskohtaisesti räätälöityä hoitoa.
Suostumukset
Kaikilta tutkittavilta pyydetään seuraavat kirjalliset suostumukset (2):
- Mikäli samalla otetaan biopankkinäytteet, pyydetään suostumus Suomen hematologinen rekisteri ja biopankki (FHRB) -tutkimukseen. Samalla tulee pyytää myös rekisterisuostumus (SHR).
- Veritautien molekylaarinen patogeneesi, altistavat tekijät ja yksilöllistetty hoito (HRUHLAB2)
Mikäli tutkittava on antanut suostumuksensa aiemmin Suomen hematologiseen rekisteriin tai FHRB-tutkimukseen, ei niiden suostumuksia tarvitse pyytää uudelleen.
FHRB-suostumusten säilytys tapahtuu siten kuin kussakin sairaalassa sovittu. Alkuperäinen HRUHLAB2-tutkimussuostumus lähetetään HYKS:iin. Suositeltavaa on myös jättää kopio omaan sairaalaan. HYKS:ssa suostumus tallennetaan FHRB-mappiin (pkl) tai osaston kanslian FHRB-laatikkoon (os 7A). Tiedotteista ja suostumuksista tulee antaa potilaalle oma kopio.
Postitusosoite HRUHLAB2 tutkimussuostumukselle:
- Eeva Lind-Ekholm, HYKS-Syöpäkeskus, Hematologian klinikka, PL 372, 00029 HUS
Näytteenotto ja lähetys
Näytteet tutkitaan Suomen molekyylilääketieteen instituutissa (FIMM) Helsingissä.
Sovi näytteenlähetyksestä Minna Suvelan tai päätutkija Caroline Heckmanin kanssa (yhteystiedot alla).
Kaikilta tutkittavilta otetaan myös ihobiopsia, jos sellaista ei FIMM:iin ole aiemmin lähetetty (myös niistä joilla FHRB-biopankkiin ihobiopsia otettu).
Yleensä näytemateriaali on luuydintä (BM), joskus myös perifeeristä verta (PB). Tutkimusnäytteistä tehdään (myeloomassa CD138-plasmasoluvalikoinnin jälkeen) eksomisekvensointi, RNA-sekvensointi sekä lääkeherkkyystutkimus. Tarvittaessa eksomisekvensointi voidaan tehdä myös muunlaisesta näytteestä (esim. ekstramedullaariset ilmentymät).
Potilaista tulisi FHRB-rekisterissä olla kirjattuna ajanmukaiset tiedot annetuista hoidoista & vasteista. Toivomme, että potilaasta otettaisiin tavanomaiset sytogeneettiset tutkimukset (esim. myeloomassa CD138-valikoiduista plasmasoluista tehtävä FISH-tutkimus) samalla kuin tutkimusnäyte ellei sitä ole parin kuukauden sisällä tehty ja tuoreimmat sytogeneettiset tulokset kirjattaisiin myös FHRB-rekisteriin.
Luuydintä kerätään myeloomassa noin 50 ml ja akuuteissa leukemioissa noin 30 ml jos halutaan tehtävän sekä lääkeherkkyysseula että sekvensointi. Pelkkään sekvensointiin riittää 20 ml luuydintä. Luuydin kerätään 10 ml EDTA putkiin (mielellään 5 ml luuydintä/putki diluution välttämiseksi). Samalla otetaan ihobiopsia (4 mm stanssibiopsia) adrenaliinia sisältävää paikallispuudutetta käyttäen (verikontaminaation vähentäminen).
Näytteenotto HYKS:ssä
- Tilaa Weblab:sta tutkimuspaketit MEKSOMISEKV_BM / MEKSOMISEKV_PB (eksomisekvensointi tai RNA-sekvensointi; luuydin tai veri), MLAAKESEU_BM / MLAAKESEU_PB (lääkeseula; luuydin tai veri), MEKSOMISEKV_SKIN (ihokoepala). Huom! eksomisekvensointinäytteen mukana aina lähetettävä myös ihobiopsia. Jos samalla otetaan FHRB-näytteet, täytyy ottaa 2 ihobiopsiaa.
- Täytä paperilähete FIMM:lle.
- HYKS:ssä näytteenoton jälkeen soita 050-44 88 032/Minna Suvela ja FIMM:stä tullaan hakemaan näyte.
Näytteen lähetys muualta kuin HYKS:stä
- Samaa paperilähetettä kuin HYKS:ssä voidaan käyttää, lähtee näytteiden mukana.
- Näyte lähetetään huoneenlämmössä ja tulisi olla perillä 24 tunnissa. On tärkeää, että näyte ei pääse jäätymään matkalla.
- FIMM voi maksaa kuljetuskulut (esim. DHL-lähettipalvelun kautta, kysy DHL-tilinumeroa FIMM:ltä ennen näytteen lähettämistä).
Sekvensointi näytteiden vastaanotto onnistuu kaikkina arkipäivinä. Sen sijaan lääkeherkkyysseulan tulokset luetaan kolmantena päivänä siitä kun syöpäsolut on altistettu lääkkeille. Jotta vältyttäisiin viikonloppuna lääkeherkkyystulosten luennalta, niin mielellään näytteet olisivat perillä maanantaina, tiistaina tai perjantai-aamupäivällä. Pyydämme huomioimaan, että FIMM:ssä ei ole virka-ajan (ma-pe klo 08-16) ulkopuolella henkilökuntaa vastaan ottamassa näytteitä ellei siitä erikseen sovita.
Näytteet käsittellään FIMM:ssä FHRB-potilasnumeron perusteella anonyymisti. Näyteputket lähetetään yleensä siten, että potilaan henkilötietotarrat oovat näyteputkissa. FIMM:ssä henkilötietotarrat hävitetään tietosuoja-asetusten mukaisesti ja vaihdetaan FHRB-numerotarroihin. Vaihtoehtoisesti näyteputket voi lähettää siten, että niihin on jo valmiiksi liimattu FHRB-numerotarrat.
Sekvensointi tehdään kiireettömästi osana prekliinistä tutkimusta tutkimusrahoituksen salliessa. Mikäli halutaan tehtäväksi kiireellinen kliininen sekvensointi (fast track) laskutetaan siitä lähettävää tahoa. Lääkeseulan tulokset valmistuvat nopeasti noin viikossa, lääkeseulatutkimuksen kustannukset laskutetaan lähettävältä taholta.
Lähetysosoite:
Caroline Heckman/ Minna Suvela
Institute for Molecular Medicine Finland FIMM
Biomedicum 2U
Tukholmankatu 8
00290 Helsinki
Yhteystiedot
Puhelin: +358 50 415 6769 (Caroline Heckman), +358 50 448 7821 (Minna Suvela)
Sähköposti: Caroline Heckman (englanniksi) ja Minna Suvela; etunimi.sukunimi@helsinki.fi
FIMM-lähete
FIMM-lähete
Sampling information
Sampling information
Here is information on sending BM or PB samples for ex vivo drug testing and molecular profiling studies at FIMM.
Prior sampling, all patients should read the HRUHLAB2 patient information sheet and sign the consent form. Original signed consent form should be sent with the sample tubes and a copy should be placed in the patient files locally.
A referral form should also be filled and sent with the samples (see attachments at the bottom of this page).
HRUHLAB3
HRUHLAB3
| Tutkimuksen vastuuhenkilöt | Prof. Kimmo Porkka, prof. Marjatta Leirisalo |
| Tutkimuksen lyhenne | HRUHLAB3 |
| Tutkimuksen suorituspaikka | HUS, hematologian ja reumatautien klinikat; Hematologinen tutkimusyksikkö (HruH); FIMM, Helsinki |
| Tutkimuksen tyyppi | Ei-kajoava laboratoriotutkimus |
| Tutkimuksen aloituspäivä | |
| Tutkimuksen status | HUS:n eettisen tmk:n hakemus submittoitu 05/2012 |
| Tutkimuspopulaatiot | Kaikki reuma- ja muita autoimmuunitauteja sairastavat potilaat |
Tutkimuksen tausta, tavoitteet ja toteutus
Kliiniseen lääkekehitysohjelmaamme liittyen totesimme, että dasatinibilääke aikaansaa potilaille samanlaisia muutoksia kuin mitä todetaan LGL-leukemiassa (klonaalisten sytotoksisten solujen ekspansio, autoimmuuni-ilmiöt). Päättelimme, että selvittämällä LGL-leukemian molekylaarisen patogeneesin ymmärtäisimme paremmin, mikä aikaansaa dasatinibilääkkeen aiheuttaman LGL-lymfosytoosin.
Teimme koko eksomin sekvensoinnin yksittäisten suomalaisten LGL-leukemiapotilaiden lymfosyyteista, joista löysimme somaattisen pistemutaation STAT3-geenissä. Löydös vahvistettiin kahdessa laajassa amerikkalaisessa LGL-potilasaineistossa. STAT3-mutaatio oli funktionaalisesti tärkeä ja siten taudin syy. Mielenkiintoista myös oli, että autimmuunitaudit, kuten nivelreuma ja immuunivälitteinen neutropenia, olivat selvästi yleisempiä STAT3-mutaatiopositiivisilla LGL-leukemia potilailla kuin mutaationegatiivisilla potilailla (Koskela ym. NEJM 2012).
Jatkuva, ligandista riippumaton STAT3-aktivaatio on todettu usean autoimmuunitaudin taustalta (mm. Crohnin ja Sjögrenin taudit), äskettäin myös varhaisessa reumataudeissa (Leirisalo-Repo ja tutk.ryhmä 2011).
Tutkimushypoteesi: lymfosyyteissä olevat somaattiset mutaatiot JAK-STAT-signaalitiessä ovat yksi autoimmuunitautien keskeinen syy
Tavoitteet: 1. Kohdennettu JAK-STAT-signaalitien keskeisten geenien mutaatioseulonta uusien, hoitamattomien reumapotilaiden eri lymfosyyttifraktioista. 2. Em. potilaiden koko eksomin ja transkriptomin syväsekvensointi 3. Reumapotilaiden lymfosyyttien repertuaarin karakterisointi syväsekvensoimalla. 4. Funktionaaliset in vitro/in vivo tutkimukset mm. spesifeillä JAK- ja STAT-inhibiittoreilla, 5. Muiden autoimmuunitautien mutaatioseulonta (mm. IBD), 6. Kohdennettujen hoitojen suunnittelu (kl. lääketutkimus).
Kyseessä on laaja 4-vuotinen yhteistyöhake HUS:n (hematologia, reumataudit, gastroenterologia), HY:n (Hematologinen tutk.yksikkö, Haartman Instituutti), sekä FIMM:in kanssa, jossa hyödynnetään alan huippuosaamista laajapohjaisesti. Mukana on myös useita koti- ja ulkomaisia yhteistyökumppaneita
Tutkimusnäytteiden otto (HUS)
Näytteenottoajat: diagnoosi- ja seurantavaiheet. Näytteenotto sovitaan aina vastuuhenkilöiden toimesta erikseen.
Verinäytteet: tutkimuspaketti xxx, tutkimusnumero xxx, 20 mL EDTA-verta. Näytteenoton jälkeen yhteys tutk.hoitaja Minna Pajuportti p. 050-427 2811
Menetelmiä
Menetelmiä
Antigeenireseptorigeeni
Antigeenireseptorigeeni
Käyttöaiheita
- Lymfaattisten maligniteettien (leukemiat, lymfoomat) diagnoosivaihe ja jäännöstautiseuranta
Tutkimusnimikkeitä
TYKS
Diagnoosivaiheessa
- 11828 Bm-ASOAL-D Immunoglobuliini ja TCR-geenit, ASO-PCR 2 klooniin, luuytimestä
- 11827 B-ASOAL-D Immunoglobuliini ja TCR-geenit, ASO-PCR 2 klooniin, verestä
Kvantitatiivinen molekulaarinen jäännöstautianalyysi seurantanäytteestä
- 12507 Bm-ASO2-QD Jäännöstautianalyysi kahteen Ig/TCR kohteeseen (kvant.), luuytimestä
- 12508 B-ASO2-QD Jäännöstautianalyysi kahteen Ig/TCR kohteeseen (kvant.), verestä
HUSLAB
- 3905 Bm-TCR-D T-solureseptorigeenin uudelleenjärjestymätutkimus, luuytimestä
- 3904 B -TCR-D T-solureseptorigeenin uudelleenjärjestymätutkimus, verestä
ISLAB
- (nimike ja linkki ohjekirjaan)
TaYS
- (nimike ja linkki ohjekirjaan)
OYS
- (nimike ja linkki ohjekirjaan)
SHR
- (tallennettavien muuttujien nimiä)
Tulkinnnassa huomioon otettavaa
- (txt)
| Kirjoittajat: | nimet |
| Viimeisin päivitys: | pvm |
| © Suomen Hematologiyhdistys | Suomen Leukemiaryhmä |
BCR-ABL1
BCR-ABL1
Käyttöaiheita
- BCR-ABL1-fuusiogeenipositiivisten tautien (KML, Ph+ALL) diagnostiikka ja jäännöstaudin seuranta
Raportointi
- Tulokset ilmoitetaan KML:n jäännöstautitutkimuksissa IS-prosenttiasteikolla
- SHR:ssa negatiivinen arvo merkitään muuttujaan b-bcr-qr-is lyhenteellä "neg" ja taudin tilanteeksi (status-cml) merkitään CMR (complete molecular response)
- Negatiivisen tuloksen yhteydessä on aina ilmoitettava myös saavutettu herkkyys; negatiivinen tulos voidaan ilmoittaa vain, jos jos näytteen herkkyys on ollut riittävä (raja-arvo 0,01%/-4,0 log/MR4)
- Herkkyys tallennetaan prosenttiarvona potilaskohtaiseen SHR-avainmuuttujaan b-bcr-qr-sens (Veren BCR-QR -tutkimuksen näytekohtainen herkkyystaso).
- Mikäli negatiiviseksi ilmoitetun näytteen herkkyys on >0,01%(MR4), näyte on tulkittava huonolaatuiseksi. Taudin tilannearviota (status-cml) ei voida tehdä. Tällöin muuttujaan b-bcr-qr-is arvo merkitään lyhenteellä "ne" (not evaluable)
Tutkimusnimikkeitä
TYKS
KML-potilailla (jäännöstautitulos IS-asteikolla)
- 12138 B-CMLPCR Kroonisen myeloisen leukemian kvantitatiivinen jäännöstautianalyysi verestä
Ph+ ALL-potilailla (jäännöstautituloksen standardina potilaan oma diagnoosivaiheen näyte)
- 4894 B-BCR-QR BCR-ABL-geenien fuusio-RNA: t(9:22), kvantitatiivinen jäännöstautianalyysi verestä
- 4895 Bm-BCR-QR BCR-ABL-geenien fuusio-RNA: t(9:22), kvantitatiivinen jäännöstautianalyysi luuytimestä
HUSLAB
- 21252 B-KML-Qr BCR/ABL-geenien fuusiotranskriptin määritys: t(9:22), kvantitatiivinen, verestä, KML-seuranta
- 4895 Bm-BCR-QR BCR/ABL-geenien fuusiotranskriptin määritys: t(9:22), kvantitatiivinen, luuytimestä, Ph+ALL- seuranta
ISLAB
- (nimike ja linkki ohjekirjaan)
Fimlab
- 4894 B-BCR-QR B -BCR/ABL-geenien fuusio-RNA: t(9;22), (kvant)
- 4895 Bm-BCR-QR Bm-BCR/ABL-geenien fuusio-RNA: t(9;22), (kvant)
NordLab
- 4894 B-BCR-Qr BCR/ABL-geenien fuusio-RNA: t(9:22), kvantitatiivinen, verestä
- 4895 Bm-BCR-Qr BCR/ABL-geenien fuusio-RNA: t(9:22), kvantitatiivinen, luuytimestä
SHR
- b-bcr-qr-is, b-bcr-qr-sens
| Kirjoittajat: | Kimmo Porkka, Perttu Koskenvesa, Veli Kairisto |
| Viimeisin päivitys: | 18.11.2010 |
| © Suomen Hematologiyhdistys | Suomen Leukemiaryhmä |
IS-standardi
IS-standardi
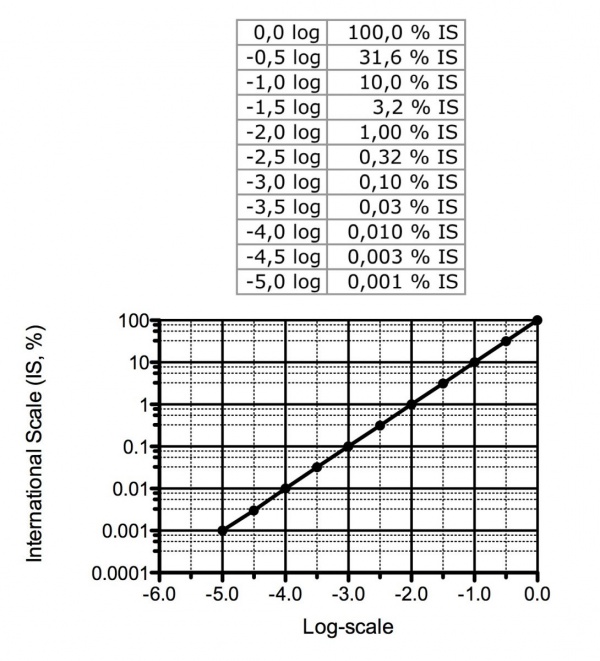
BCR-ABL1-transkriptiarvojen raportoinnissa käytetään KML:ssä International Scale (IS) -asteikkoa.
Tuloksen ilmoittaminen IS-asteikolla vaatii laboratoriolta standardointikierrosten avulla lasketun korjauskertoimen säännöllistä päivittämistä. FIMLAB käyttää Ipsogenin systeemiä, jossa on plasmidistandardi ja kittikohtainen IS- kalibraatioarvo tuloksen ilmoittamiseksi IS- asteikolla.
Vanhat log-arvot vertautuvat prosenttilukuihin oheisen taulukon ja kaavakuvan mukaisesti (ei tarkka muutos, menetelmäriippuvainen).
MR3 ≤ 0.1%, MR4 ≤ 0.01%, MR4.5 ≤ 0.0032%, MR5 ≤ 0.001%
CEBPA
CEBPA
Käyttöaiheita
- Akuutin leukemian diagnostiikka ja jäännöstaudin seuranta
Raportointi
- Tulokset ilmoitetaan prosenttilukuna suhteutettuna kontrolligeenin ilmentymään
- Negatiivinen tulos ilmoitetaan arvolla 0,0001% (=-6 log). SHR:ssa negatiivinen arvo merkitään lyhenteellä "neg". Negatiivisen tuloksen yhteydessä on aina ilmoitettava myös saavutettu herkkyys; negatiivinen tulos voidaan ilmoittaa vain, jos jos näytteen herkkyys on ollut riittävä (raja-arvo x.xx).
Tutkimusnimikkeitä
TYKSLAB
- (nimike ja linkki ohjekirjaan)
HUSLAB
- (nimike ja linkki ohjekirjaan)
ISLAB
- (nimike ja linkki ohjekirjaan)
TaYS
- (nimike ja linkki ohjekirjaan)
OYS
- (nimike ja linkki ohjekirjaan)
SHR
- (tallennettavien muuttujien nimiä)
Tulkinnnassa huomioon otettavaa
- (txt)
| Kirjoittajat: | Kimmo Porkka |
| Viimeisin päivitys: | 31.05.2010 |
| © Suomen Hematologiyhdistys | Suomen Leukemiaryhmä |
FLT3
FLT3
Käyttöaiheita
- Akuutin leukemian diagnostiikka ja jäännöstaudin seuranta
Raportointi
- Tulokset ilmoitetaan prosenttilukuna suhteutettuna kontrolligeenin ilmentymään
- Negatiivinen tulos ilmoitetaan arvolla 0,0001% (=-6 log). SHR:ssa negatiivinen arvo merkitään lyhenteellä "neg". Negatiivisen tuloksen yhteydessä on aina ilmoitettava myös saavutettu herkkyys; negatiivinen tulos voidaan ilmoittaa vain, jos jos näytteen herkkyys on ollut riittävä (raja-arvo x.xx).
Tutkimusnimikkeitä
TYKS
Diagnoosivaiheen näytteestä
- 11191 Bm-FLT3-D FLT3-geenin mutaatiohaku, luuytimestä
- 11192 B-FLT3-D FLT3-geenin mutaatiohaku, verestä
- 11193 Bm-FLT3sek FLT3-geenin sekvenssianalyysi ASO-aluketta varten, luuytimestä
- 11194 B-FLT3sek FLT3-geenin sekvenssianalyysi ASO-aluketta varten, verestä
Kvantitatiivinen jäännöstautianalyysi seurantanäytteestä
- 12487 Bm-FLT3-QD FLT3-geenin kvantitatiivinen mutaatioanalyysi, luuytimestä
- 12486 B-FLT3-QD FLT3-geenin kvantitatiivinen mutaatioanalyysi, verestä
HUSLAB
- (nimike ja linkki ohjekirjaan)
ISLAB
- (nimike ja linkki ohjekirjaan)
TaYS
- (nimike ja linkki ohjekirjaan)
OYS
- (nimike ja linkki ohjekirjaan)
SHR
- (tallennettavien muuttujien nimiä)
Tulkinnnassa huomioon otettavaa
- (txt)
| Kirjoittajat: | Kimmo Porkka |
| Viimeisin päivitys: | 31.05.2010 |
| © Suomen Hematologiyhdistys | Suomen Leukemiaryhmä |
Fuusiogeeniseulonta
Fuusiogeeniseulonta
Käyttöaiheita
- Akuutin leukemian diagnostiikka
Raportointi
- Tulokset ilmoitetaan lausuntomuotoisena
Tutkimusnimikkeitä
TYKS
- 12494 Bm-Fuus-mR Hematologinen fuusiogeeniseulonta, luuytimestä
- 12495 B-Fuus-mR Hematologinen fuusiogeeniseulonta, verestä
HUSLAB
- 8906 Bm-Fuus-mR Hematologinen fuusiogeeniseulonta, luuytimestä
- 8905 B -Fuus-mR Hematologinen fuusiogeeniseulonta, verestä
ISLAB
- (nimike ja linkki ohjekirjaan)
TaYS
- (nimike ja linkki ohjekirjaan)
OYS
- (nimike ja linkki ohjekirjaan)
SHR
- (tallennettavien muuttujien nimiä)
Tulkinnnassa huomioon otettavaa
- (txt)
| Kirjoittajat: | Kimmo Porkka |
| Viimeisin päivitys: | 31.05.2010 |
| © Suomen Hematologiyhdistys | Suomen Leukemiaryhmä |
JAK2
JAK2
Käyttöaiheita
- (teksti)
Tutkimusnimikkeitä
TYKS
Myeloproliferatiivisen taudin diagnostiikka
- 4952 B-JAK2-D JAK2-geenin mutaatioanalyysi, verestä
- 11937 Bm-JAK2-D JAK2-geenin mutaatioanalyysi, luuytimestä
- 12662 B-JAK2-QD JAK2-geenin kvantitatiivinen mutaatioanalyysi, verestä
- 12663 Bm-JAK2-QD JAK2-geenin kvantitatiivinen mutaatioanalyysi, luuytimestä
HUSLAB
- (nimike ja linkki ohjekirjaan)
ISLAB
- (nimike ja linkki ohjekirjaan)
TaYS
- (nimike ja linkki ohjekirjaan)
OYS
- (nimike ja linkki ohjekirjaan)
SHR
- (tallennettavien muuttujien nimiä)
Tulkinnnassa huomioon otettavaa
- (txt)
| Kirjoittajat: | Kimmo Porkka |
| Viimeisin päivitys: | 31.05.2010 |
| © Suomen Hematologiyhdistys | Suomen Leukemiaryhmä |
NPM1
NPM1
Käyttöaiheita
- Akuutin leukemian ja MDS:n diagnostiikka ja jäännöstaudin seuranta
Tutkimusnimikkeitä
TYKS
- 11935 Bm-NPM1-D Nukleofosmiinigeenin mutaatioanalyysi, luuytimestä
- 11936 B-NPM1-D Nukleofosmiinigeenin mutaatioanalyysi, verestä
- 13118 Ts-NPM1-D Nukleofosmiinigeenin mutaatioanalyysi, kudoksesta
- 12489 Bm-NPM1-QD Nukleofosmiinigeenin kvantitatiivinen mutaatioanalyysi, luuytimestä
- 12488 B-NPM1-QD Nukleofosmiinigeenin kvantitatiivinen mutaatioanalyysi, verestä
HUSLAB
- (nimike ja linkki ohjekirjaan)
ISLAB
- (nimike ja linkki ohjekirjaan)
TaYS
- (nimike ja linkki ohjekirjaan)
OYS
- (nimike ja linkki ohjekirjaan)
SHR
- (tallennettavien muuttujien nimiä)
Tulkinnnassa huomioon otettavaa
- (txt)
| Kirjoittajat: | Kimmo Porkka |
| Viimeisin päivitys: | 31.05.2010 |
| © Suomen Hematologiyhdistys | Suomen Leukemiaryhmä |
Ohjeita
Ohjeita
Haittavaikutusten raportointi
Haittavaikutusten raportointi
Sairauteen tai hoitoihin liittyvien haittavaikutusten kirjaamisessa noudatetaan CRF-lomakkeiden käytäntöä. Suosituksena on kirjata haittavaikutukset CTC-koodiston mukaisesti. Pikaopas (pdf-tiedosto).