AML-2012 (vanha protokolla)
- Kirjaudu tai rekisteröidy kommentoidaksesi
AML-2012 (vanha protokolla)
Täältä löydät tietoa Suomen leukemiaryhmän AML-2012-hoito-ohjelmasta (lopullisen version päiväys 11.01.2012). Se on kokonaisuudessaan ladattavissa alla olevasta liitetiedostosta (attachment). Alla otsikoittain jaoteltuna on esitetty keskeiset osiot hoito-ohjelmasta.
Tiivistelmä AML-2012
- Kirjaudu tai rekisteröidy kommentoidaksesi
Tiivistelmä AML-2012
Kyseessä on 16-vuotiaille ja sitä vanhemmille akuuttia myelooista leukemiaa (AML) sairastaville potilaille tarkoitettu valtakunnallinen Suomen leukemiaryhmän (SLR) laatima hoito-ohjelma, jonka tarkoitus on saada kaikki yli 65-vuotiaat potilaat yhtenäisen hoidon piiriin.
Hoito-ohjelmaan soveltuva potilas saa aluksi induktiohoidon (enimmillään kaksi sykliä), jolla tähdätään morfologiseen remissioon. Remissio pyritään mahdollisuuksien mukaan arvioimaan luuydinnäytteestä myös virtaussytometrisellä menetelmällä. Morfologisen remission saavuttaneet potilaat jaetaan kolmeen eri riskiluokkaan (pieni riski, keskiriski ja suuri riski) dg-vaiheessa otettujen geneettisten tutkimustulosten mukaisesti. Jokaisessa riskiluokassa toteutetaan remission jälkeen konsolidaationa enimmillään kolme solunsalpaajahoitoa, jonka jälkeen siirrytään seurantaan. Kuitenkin kaikille niille remission saavuttaneille allogeeniseen siirtoon soveltuville keskiriskin ja suuren riskin potilaille, joille sopiva luovuttaja löytyy, suositellaan ensimmäisessä remissiossa konsolidaationa allogeenista kantasolusiirtohoitoa heti kun se on mahdollista toteuttaa. Pienen riskin potilaille suositellaan allogeenista kantasolusiirtohoitoa ensimmäisessä remissiossa vain, jos kolmen konsolidaatiohoidon jälkeen heillä on molekulaarisesti mitattava merkittävä jäännöstauti.
Jäännöstautia seurataan allogeeniseen kantasolusiirtohoitoon soveltuvilla geneettisesti pienen riskin potilailla jokaisen hoidon jälkeen ja seurantavaiheessa kolmen kuukauden välein kahteen vuoteen saakka remission toteamisesta. Jos tällaiselle potilaalle ilmaantuu seurannan aikana merkittävä jäännöstauti, hänelle suositellaan allogeenista kantasolusiirtohoitoa, jos se on mahdollista toteuttaa. Muissa riskiryhmissä jäännöstaudin seuranta ei ole välttämätön, mutta sitä suositellaan tehtäväksi kuten pienen riskin ryhmässä, tutkimustiedon kartuttamiseksi tulevia hoitotutkimuksia ajatellen. Pienen riskin potilaille jäännöstaudin seurantaan soveltuvin menetelmä on RQ-PCR. Muissa riskiryhmissä jäännöstaudin seurantaan käytetään soveltuvinta herkintä menetelmää. Jäännöstaudin seurantaa suositellaan tehtäväksi myös virtaussytometrialla.
Induktiohoidolle refraktaaristen ja hoidon tai seurannan aikana relaboituvien potilaiden jatkohoidosta päättää hoitava lääkäri.
Potilaat ja hoitotulosten arvioimisessa tarvittavat seurantatiedot (erillinen raportointiliite) ilmoitetaan potilaan antamalla kirjallisella suostumuksella Suomen Hematologiseen Rekisteriin (SHR). Jokainen vastuulääkäri ohjeistaa ERVA-alueensa keskussairaalat hoito-ohjelman ja sen raportoinnin suhteen.
Hoito-ohjelmassa mukana oleville potilaille suositellaan osallistumista mahdollisesti myöhemmin käynnistyviin erillisiin SLR:n suunnittelemiin AML:n tutkimuksiin.
Hoito-ohjelmaan pyritään saamaan 400 potilasta vuosien 2012 - 2015 aikana.
Vuokaaviot (AML-2012)
- Kirjaudu tai rekisteröidy kommentoidaksesi
Vuokaaviot (AML-2012)
AML-2012-hoito-ohjelma: yleiskaavio
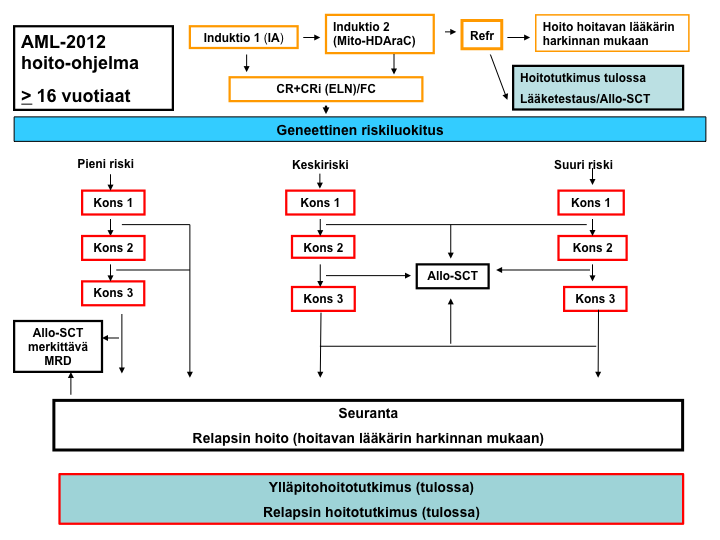
Pienen relapsiriskin hoitokaavio
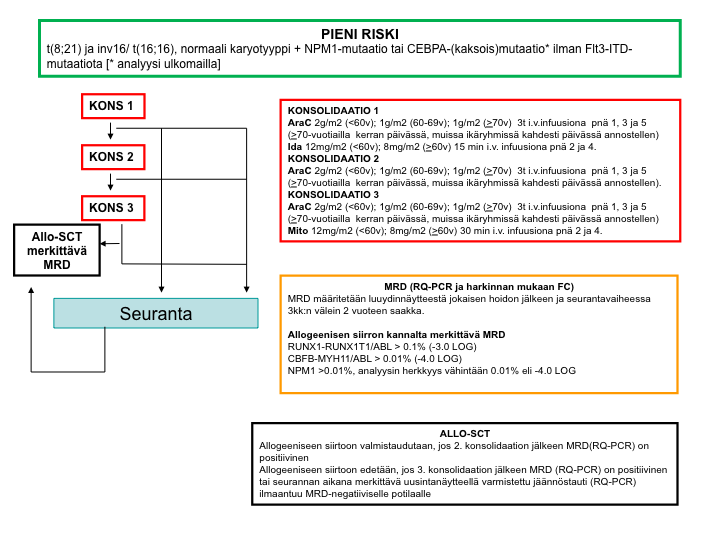
Keskisuuren relapsiriskin hoitokaavio
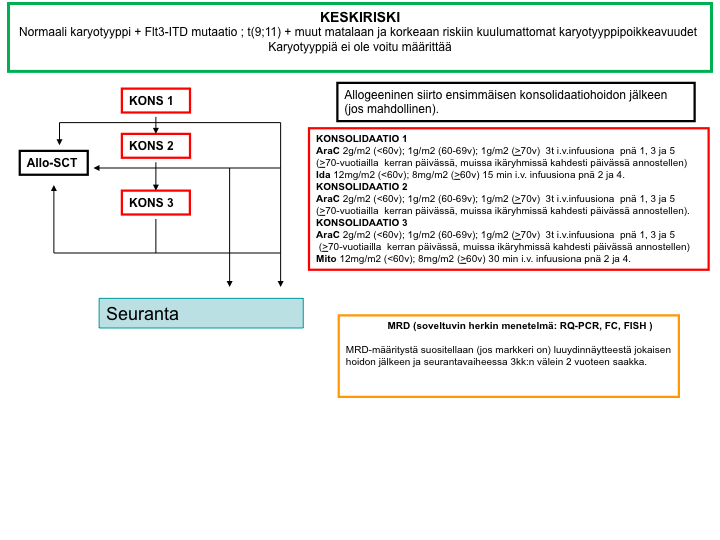
Suuren relapsiriskin hoitokaavio
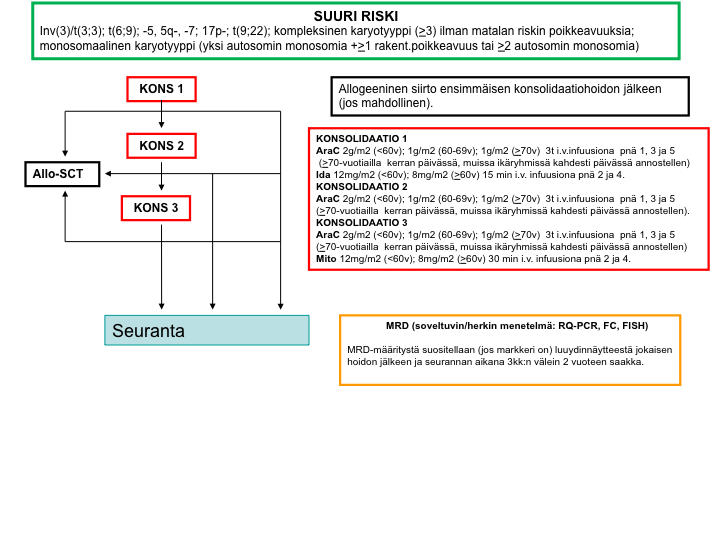
Valintakriteerit
- Kirjaudu tai rekisteröidy kommentoidaksesi
Valintakriteerit
- Potilaan ikä on dg-hetkellä >16 vuotta
- Potilaalla on AML WHO-kriteerien mukaisesti
- Allekirjoitettu kirjallinen suostumus tietojen tallentamisesta Suomen Hematologiseen Rekisteriin (FHRB)
Poissulkukriteerit
- Akuutti promyelosyyttileukemia
- Soveltumattomuus hoito-ohjelmaan: vaikea sydän-, keuhko-, maksa- tai munuaissairaus, vaikea psykiatrinen sairaus/tila, vaikea dementia, huono hoitomyöntyvyys
- Arvioitu elinaika leukemiasta riippumattomasta syystä on alle 6 kk.
Hoito-ohjelman ensisijaiset päätetapahtumat
- Remissio (CR)
- Relapsivapaa elinaika (RFS)
- Kumulatiivinen relapsin insidenssi (CIR)
- Kokonaiselinaika
Hoito-ohjelman toissijaiset päätetapahtumat
- Induktio- ja konsolidaatiohoidon kuolleisuus
- Hoitosyklin viivästymisen syyt
- Hoito-ohjelman keskeyttämisen syyt
Muita raportoitavia parametreja
Jokaisesta hoitosyklistä:
- Neutropenian kesto (<0.5)
- Trombosytopenian kesto (<50)
- Infektioiden vaikeusaste (WHO-luokitus)
- Veriviljelypositiiviset infektiot
- Sairaalapäivät
- Jäännöstaudin määrä
Seurantavaihe:
- Jäännöstaudin määrä 3 kk välein 2 vuoteen saakka
Induktiohoidot (AML-2012)
- Kirjaudu tai rekisteröidy kommentoidaksesi
Induktiohoidot (AML-2012)
Ensimmäinen induktio (IA)
Idarubisiini (Ida): 12 mg/m2 päivinä 1, 3 ja 5 15 min iv infuusiona (sama annos kaikissa ikäryhmissä)
Sytarabiini (AraC):
• <60-vuotiaat: bolus 100 mg päivänä 1 ja 100 mg/m2 jatkuvana iv infuusiona pnä 1-9
• ≥60-vuotiaat: bolus 100 mg päivänä 1 ja 100 mg/m2 jatkuvana iv infuusiona pnä 1-7
Toinen induktio (Mito-HDAraC)
Se annetaan vain, jos potilas ei mene morfologiseen remissioon ensimmäisellä induktiolla.
Mitoksantroni (Mito):
• <60-vuotiaat: 12 mg/m2 30 min iv. infuusiona pnä 2-5
• ≥60-vuotiaat: 8 mg/m2 30 min iv. infuusiona pnä 2-5
Suuriannos-sytarabiini (HDAraC):
• <60-vuotiaat: 2 g/m2 3 tunnin iv. infuusiona 12 tunnin välein päivinä 1, 3, 5 ja 7
• 60-69-vuotiaat: 1 g/m2 3 tunnin iv. infuusiona 12 tunnin välein päivinä 1,3, 5 ja 7
• ≥70-vuotiaat: 1 g/m2 3 tunnin iv. infuusiona kerran päivässä päivinä 1, 3, 5 ja 7
• Oftan Dexa silmätipat 1gttx4-6 molempiin silmiin pnä 1-8
Konsolidaatiohoidot (AML-2012)
- Kirjaudu tai rekisteröidy kommentoidaksesi
Konsolidaatiohoidot (AML-2012)
Ensimmäinen konsolidaatiohoito (HDAraC-Ida)
Annetaan vain, jos potilas saavuttaa morfologisen remission joko ensimmäisellä tai toisella induktiohoidolla.
Suuriannos-sytarabiini (HDAraC):
• <60-vuotiaat: 2 g/m2 3 tunnin iv. infuusiona 12 tunnin välein pnä 1, 3 ja 5
• 60-69-vuotiaat: 1 g/m2 3 tunnin iv infuusiona 12 tunnin välein pnä 1, 3 ja 5
• ≥70-vuotiaat: 1 g/m2 3 tunnin iv. infuusiona kerran päivässä pnä 1, 3 ja 5
• deksametasoni-silmätipat 1 gtt x4-6 molempiin silmiin pnä 1-6
Idarubisiini:
• <60-vuotiaat: 12 mg/m2 15 min iv. infuusiona pnä 2 ja 4
• ≥60-vuotiaat: 8 mg/m2 15 min iv. infuusiona pnä 2 ja 4
Toinen konsolidaatiohoito (HDAraC)
Se annetaan vain, jos potilas on morfologisessa remissiossa.
Suuriannos-sytarabiini (HDAraC):
• <60-vuotiaat: 2 g/m2 3 tunnin iv. infuusiona 12 tunnin välein pnä 1, 3 ja 5
• 60-69-vuotiaat: 1 g/m2 3 tunnin iv infuusiona 12 tunnin välein pnä 1, 3 ja 5
• ≥70-vuotiaat: 1 g/m2 3 tunnin iv. infuusiona kerran päivässä pnä 1, 3 ja 5
• deksametasoni-silmätipat 1 gtt x4-6 molempiin silmiin pnä 1-6
Kolmas konsolidaatiohoito (HDAraC-Mito)
Se annetaan vain, jos potilas on morfologisessa remissiossa.
Suuriannos-sytarabiini (HDAraC):
• <60-vuotiaat: 2 g/m2 3 tunnin iv. infuusiona 12 tunnin välein pnä 1, 3 ja 5
• 60-69-vuotiaat: 1 g/m2 3 tunnin iv infuusiona 12 tunnin välein pnä 1, 3 ja 5
• ≥70-vuotiaat: 1 g/m2 3 tunnin iv. infuusiona kerran päivässä pnä 1, 3 ja 5
• deksametasoni-silmätipat 1 gtt x4-6 molempiin silmiin pnä 1-6
Mitoksantroni (Mito):
• <60-vuotiaat: 12 mg/m2 30 min iv. infuusiona pnä 2 ja 4
• ≥60-vuotiaat: 8 mg/m2 30 min iv. infuusiona pnä 2 ja 4
Kantasolujensiirto (kriteerit AML-2012)
- Kirjaudu tai rekisteröidy kommentoidaksesi
Kantasolujensiirto (kriteerit AML-2012)
Pienen riskin AML-potilailla valmistaudutaan kolmannen hoidon jälkeen tehtävään allogeeniseen kantasolusiirtohoitoon, jos aikaisempien hoitojen jäännöstaudin perusteella se näyttää todennäköiseltä. Jos siirto ei ole mahdollinen, siirrytään seurantavaiheeseen.
Keskisuuren ja suuren riskin ryhmässä tehdään allogeeninen kantasolujensiirto kahden hoidon jälkeen tai sen jälkeen heti kun se on mahdollista, jos sopiva luovuttaja (sisarus tai rekisteristä peräisin oleva) on olemassa ja siirto muutoin on mahdollista toteuttaa. Jos luovuttajaa ei ole, annetaan potilaille yhteensä kolme konsolidaatiota. Kolmen konsolidaatiohoidon jälkeen tai konsolidaatiohoitojen keskeytyessä siirrytään seurantavaiheeseen.
Allogeenista kantasolujensiirtohoitoa tarjotaan edellä esitetyin perustein siirtoon soveltuvalle potilaalle 65 ikävuoteen saakka ja yksilöllistä harkintaa käyttäen aina 70 ikävuoteen saakka, jos hänelle löytyy sopiva luovuttaja. Siirtoon soveltuvista keskiriskin ja suuren riskin potilaista laaditaan lähete allogeeniseen siirtoyksikköön (HYKS tai TYKS) mahdollisimman varhaisessa vaiheessa. Myös pienen riskin potilaiden siirtoon varaudutaan mahdollisimman varhain jäännöstaudin tulos huomioiden. Lähetteeseen liitetään liitteen 7 mukaiset tiedot (ks. erillinen linkki ja protokolla). Jos sisarusluovuttajaa ei löydy, siirtokeskus ryhtyy etsimään rekisteriluovuttajaa. Samanaikaisesti tiiviisti seurataan potilaan hoidon etenemistä ja mahdollisten komplikaatioiden syntymistä. Jos potilaalle löytyy sisarusluovuttaja tai rekisteristä löytyy kudostyypiltään sopiva luovuttaja (siirtokeskuksen tekemä valinta), käydään siirtokeskuksessa keskustelu allogeeniseen siirtoon liittyvistä asioista potilaan, lähiomaisen ja mahdollisen sisarusluovuttajan kesken. Kun potilas on ilmoittanut keskustelun jälkeen haluavansa edetä siirtoon (ja sisarusluovuttaja samoin), voidaan tautitilanteen salliessa ryhtyä aktivoimaan siirtoaikataulua. Noin kolme viikkoa ennen kantasolujen siirtopäivää potilas ja sisarusluovuttaja tutkitaan polikliinisesti siirtoyksikössä. Mikäli tutkimuksissa ei ilmene estettä, edetään suunniteltuun intensiivihoitoon. Rekisterin luovuttaja tutkitaan rekisterin toimesta. Lopullisen arvion potilaan sopivuudesta siirtoon, luovuttajan valinnan ja potilaalle annettavan esihoidon tekee siirtoyksikkö.
Keskiriskin ja suuren riskin potilailla siirtoon pääsyn optimaalisin ajankohta on induktion tai yhden konsolidaation jälkeen.
Tietojen rekisteröinti
- Kirjaudu tai rekisteröidy kommentoidaksesi
Tietojen rekisteröinti
Hoito-ohjelman tiedot ovat SLR:n omaisuutta. Raportoitavat tiedot siirretään potilaan kirjallisella suostumuksella Suomen Hematologiseen Rekisteriin (SHR/FHRB). Raportoitavat tiedot voidaan siirtää joko suoraan rekisteriin tai ne voidaan ensin kerätä erillisille kaavakkeille ja niistä myöhemmin siirtää rekisteriin. Tietojen siirtäminen rekisteriin edellyttää sitä, että SHR on hyväksytty sairaanhoitopiireissä käyttöön (eettisen toimikunnan kannanotto ja shp:n johtajaylilääkärin hyväksyntä). Jokaisen ERVA-alueen vastuulääkäri huolehtii siitä, että SHR on saanut hyväksynnän alueellaan. Hän myös ohjeistaa tietojen keräämisen vastuualueellaan. Kerättyjä tietoja käsitellään salassa pidettävien tietojen vaatimusten mukaisesti. Vain nimettyjen henkilöiden on mahdollista tarkastella hoitotuloksia. SHR:n tiedoista tehdyistä yhteenvedoissa ja raporteissa yksittäisten potilaiden tietoja ei voida tunnistaa.
Allogeenisen kantasolusiirtohoidon saaneet potilaat raportoidaan tästä riippumatta transplantaatiorekistereihin normaalin käytännön mukaisesti ja tuloksia voidaan käyttää rekisterien tekemissä analyyseissä. Hoito-ohjelman tuloksista raportoidaan leukemiaryhmälle ja ne hyödynnetään niissä erillisissä hoitotutkimuksissa, joihin potilaita tästä hoito-ohjelmasta mahdollisesti suositellaan. Hoitotulokset pyritään myös raportoimaan alan kansainvälisissä lehdissä SLR:n toimesta. SLR päättää julkaisujen kirjoittajista erikseen.
Vastuulääkärit
- Kirjaudu tai rekisteröidy kommentoidaksesi
Vastuulääkärit
Pirjo Koistinen
AML-2012-hoito-ohjelman vastuuhenkilö
Syöpätaudit ja hematologia, Medisiininen tulosalue, OYS
PL 20, 90029 OYS
pirjo.koistinen@ppshp.fi, puh (08) 315 4617
Kimmo Porkka
Hematologian klinikka, Medisiininen tulosyksikkö, HYKS
PL 372, Haartmaninkatu 4, 00029 HUS
kimmo.porkka@helsinki.fi, puh. 09 471 72338
Tapio Nousiainen
Sisätautien klinikka, KYS
PL 1777, 70211 Kuopio
tapio.nousiainen@kuh.fi, puh. (017) 173 311
Maija Itälä-Remes
osasto 015, TYKS
PL52, 20521 Turku
maija.itala-remes@tyks.fi, puh (02) 313 0000
Hannele Rintala
Sisätautien klinikka, TAYS
PL 2000, 33521 Tampere
hannele.rintala@pshp.fi, puh (03) 311 611
Potilaan tiedote
- Kirjaudu tai rekisteröidy kommentoidaksesi
Potilaan tiedote
Versio 17.04.2012
Tietoa akuutista myelooisesta leukemiasta ja sen uudesta suomalaisesta hoito-ohjelmasta
16-VUOTIAIDEN JA SITÄ VANHEMPIEN AKUUTTIA MYELOOISTA LEUKEMIAA SAIRASTAVIEN POTILAIDEN HOITO-OHJELMA
Lyhenne: AML-2012
Arvoisa potilas
Tässä tiedotteessa kerrotaan akuutin myelooisen leukemian uudesta hoito-ohjelmasta, jonka piiriin pyritään saamaan mahdollisimman moni kyseiseen leukemiaan sairastuva aikuispotilas Suomessa. Hoito-ohjelma on Suomen Leukemiaryhmän laatima ja siinä hyödynnetään viimeaikaisin tutkimustieto taudista ja sen hoidosta.
Akuutin myelooisen leukemian hoidon yleisiä periaatteita
Akuutti myelooinen leukemia on aikuisten yleisin akuutti leukemia, jossa luuydin tuottaa epäkypsiä blastisoluja (leukemiasoluja) verenkiertoon, josta ne voivat levitä muualle elimistöön. Samanaikaisesti luuytimen normaali verisolumuodostus estyy ja aiheuttaa anemian, terveiden valkosolujen vähyyden ja verihiutaleiden kadon. Terveiden valkosolujen vähyys johtaa toistuviin infektioihin ja verihiutaleiden eli trombosyyttien kato lisää verenvuotoja. Veren suuri blastimäärä voi johtaa verenkiertohäiriöihin ja eri elinten normaalin toiminnan häiriintymiseen. Hoitamattomana tauti johtaa nopeasti kuolemaan.
Akuutin myelooisen leukemian hoidon kulmakivi on suuriannoksinen solunsalpaajalääkitys, joita annetaan muutaman päivän kuureina 4 – 6 viikon välein. Yleensä hoitokuureja tarvitaan useita. Hoidon päämääränä on taudista paraneminen, johon päästään tuhoamalla kaikki elimistössä olevat leukemiasolut.
Leukemian hoidot aiheuttavat veren kaikkien soluarvojen voimakkaan mutta ohimenevän laskun, mikä selittää suuren osan hoitoon liittyvistä haittavaikutuksista. Haittavaikutuksina voi esiintyä väsymystä, tulehduksia ja verenvuotoja. Suun kipeytyminen, ruokahaluttomuus, pahoinvointi, ripuli ja hiusten lähtö ovat myös tavallisia. Mahdollisuus lasten saamiseen huononee hoitojen takia.
Suurin osa haittavaikutuksista on kuitenkin pääsääntöisesti hoidettavissa tukihoidoin. Tukihoitoina tarvitaan verituotteita ja antibiootteja, joita annetaan toistuvasti laskimonsisäisesti. Hoitojen aikana joudutaan turvautumaan usein myös suonensisäiseen ravitsemushoitoon. Hoitojen helpottamiseksi tarvitaan lähes poikkeuksetta keskuslaskimokatetria, jonka anestesialääkäri laittaa paikallispuudutuksen avulla suureen laskimoon. Katetri on tarkoitettu pitkäaikaiseen käyttöön, eikä se estä esimerkiksi kotona käymistä hoitojen välissä.
Ensimmäisellä hoitojaksolla pyritään saavuttamaan remissio, jolloin leukemiasoluja ei enää nähdä luuytimessä, veriarvot ovat normaalistuneet ja leukemian mahdollisesti aiheuttamat oireet ovat hävinneet. Myöhempien hoitojaksojen tarkoituksena on hävittää mahdollinen mikroskoopilla havaitsematon jäännöstauti ja estää taudin uusiutuminen eli relapsi.
Normaalin käytännön mukaisesti hoidon tuloksia seurataan veri- ja luuydinnäytteiden avulla. Verinäytteitä otetaan voimakkaiden hoitojen jälkeen lähes päivittäin. Luuydinnäytteitä tutkitaan noin kuukauden kuluttua ensimmäisen hoidon alusta ja myöhemmin hoitokuurien jälkeen veriarvojen toivuttua sekä seurantavaiheessa neljä kertaa vuodessa kahden vuoden ajan. Kantasolujensiirron hyödyistä ja riskeistä järjestetään erillinen keskustelu niille potilaille, jotka ovat siihen soveliaita ja joille tätä hoitomuotoa tarjotaan 1 – 3 solunsalpaajakuurin jälkeen.
Hoitokuurit annetaan yleensä sairaalassa. Infektioiden ja verenvuotojen vaaran takia joudutaan hoitokuurien jälkeen olemaan sairaalassa yleensä muutamia viikkoja. Sairaalahoitojaksojen välillä lyhyet kotilomat ovat usein mahdollisia.
Hoito-ohjelman suunnittelija – Suomen Leukemiaryhmä
Maassamme akuuttien leukemioiden hoito ohjelmat on suunniteltu yli 25 vuoden ajan Suomen Leukemiaryhmän toimesta. Ryhmään kuuluu lääkäreitä pahanlaatuisia veritauteja hoitavista sairaaloista. Yhteisen suunnittelun ja tulosten seuraamisen tarkoituksena on kehittää Suomen oloihin parhaiten soveltuvia ja tehokkaita hoito ohjelmia. Käsillä oleva hoito-ohjelma toteutetaan kaikissa Suomen yliopistollisissa sairaaloissa ja joissakin keskussairaaloissa. Tähän mennessä toteutetuilla hoito- ja tutkimusohjelmilla saavutetut hoitotulokset ovat parantuneet koko ajan ja ovat myös kansainvälisesti arvioituna korkeatasoisia.
Miksi tämä hoito-ohjelma on laadittu?
Leukemian hoidossa käytetään monenlaisia solunsalpaajahoitojen yhdistelmiä, joilla on saavutettu kohtalaisen hyviä hoitotuloksia. Tällä hetkellä ei voida sanoa mikä yhdistelmistä on kaikkein paras. Tämän takia yksityiskohdiltaan toisistaan eroavia hoito-ohjelmia on syytä edelleen arvioida niin tehon kuin haittavaikutustenkin suhteen.
Tässä hoito-ohjelmassa kaikki potilaat saavat saman remissioon tähtäävän induktiohoidon sekä remission saavuttamisen jälkeen kolme konsolidaatiohoitoa taudin uusiutumisen estämiseksi. Potilaat jaetaan tiettyjen diagnoosivaiheessa todettujen riskitekijöiden perusteella kolmeen eri riskiluokkaan, mikä vaikuttaa siihen, suositellaanko etenemistä allogeeniseen kantasolusiirtoon, jos sopiva kantasolujen luovuttaja löytyy.
Akuutin myelooisen leukemian ennuste vaihtelee potilaittain huomattavasti. Diagnoosivaiheen löydösten perusteella hoitovasteen saannin mahdollisuutta ja leukemian uusiutumisen riskiä voidaan arvioida monin tavoin. Viime vuosina sairaalakäyttöön on kehitetty aiempaa herkempiä menetelmiä elimistöön hoidon jälkeen mahdollisesti jäävien leukemiasolujen eli jäännöstaudin toteamiseksi. Herkät tutkimusmenetelmät ovat tuoneet runsaasti uutta tietoa leukemian hoitoon, mutta niihin liittyy myös runsaasti selvitettäviä kysymyksiä sekä laboratoriotekniikan että tulosten arvioinnin kannalta. Tässä hoito-ohjelmassa nämä riskitekijät kartoitetaan uusien kansainvälisten ohjeiden mukaisesti ja mahdollista jäännöstautilöydöstä pyritään seuraamaan luuydinnäytteestä säännöllisin väliajoin aina 2 vuoteen saakka sairastumisesta.
Hoito-ohjelman tavoite
Hoitojen jatkuvan kehittämisen takia on tärkeää kerätä tiedot paitsi hoitotuloksista myös leukemian luonteesta ja potilaskohtaisista hoidon tuloksiin vaikuttavista tekijöistä. Ohjelmaan pyritään saamaan kaikki Suomessa hoidettavat 16-vuotiaat ja sitä iäkkäämmät voimakkaaseen solunsalpaaja-hoitoon soveltuvat akuuttia myelooista leukemiaa sairastavat potilaat. Hoitoon soveltuvuuttaa arvioidaan aikaisempaa paremmin hyödyntäen WHO:n toimintakykymittaristoa sekä muun sairastavuuden pisteytystä siihen kehitetyillä ohjeistuksilla.
Hoito-ohjelman tärkeä tavoite on saada myös iäkkäät potilaat parantavan hoidon piiriin ja samalla arvioida, parantaako voimakas hoito iäkkäiden potilaiden ennustetta, ja onko hoidon toksisuus hyväksyttävissä. Alle 65-vuotiaiden kohdalla hoitotuloksia voidaan verrata historiallisiin kontrolleihin eli AML-92 ja AML-03-hoitotutkimuksiin osallistuneiden potilaiden hoitotuloksiin.
Tässä hoito-ohjelmassa potilaiden ohjaaminen allogeeniseen kantasolusiirtohoitoon nopeutuu ja tehostuu. Samalla kaikki (myös iäkkäät) yleisten suositusten mukaan allogeenisen kantasolusiirtohoidon piiriin kuuluvat potilaat saadaan systemaattisesti poimittua siirto-ohjelmaan.
Hoito-ohjelman yksi tavoite on arvioida jäännöstaudin merkitys kaikissa riskiryhmissä potilaan ennusteeseen. Tässä hoito-ohjelmassa tätä tietoa kerätään entistä systemaattisemmin ja useammalla eri menetelmällä. Tieto voidaan hyödyntää tulevaisuudessa arvioitaessa sitä, missä vaiheessa ja minkä suuruinen jäännöstauti tulisi hoitoa tehostamalla pyrkiä eliminoimaan.
Diagnoosi-, remissio- ja mahdollisessa relapsivaiheessa kerättävät veri- ja luuydinnäytteet, sekä kliinisen tiedon keräys Suomen hematologiseen rekisteriin ja biopankkiin (FHRB) mahdollistavat akuutin leukemian hoidon jatkuvan kehitystyön. Rekisteriin kerätty data helpottaa ja nopeuttaa hoito-ohjelman tulosten tilastollista analysointia ja väliraporttien tekemistä. Tästä tutkimuksesta saatte erillisen tiedotteen ja suostumuskaavakkeen.
Teiltä pyydetään kirjallinen suostumus biopankkinäytteiden ottamiseen sekä hoitotietojen siirtämiseen ja raportointiin Suomen Hematologiseen Rekisteriin. Mahdollinen kieltäytymisenne tietojenne rekisteröinnistä tai tutkimusnäytteiden otosta ei vaaranna tautinne hoitoa tämän hoito-ohjelman tai muun tunnetun hoito-ohjeistuksen mukaisesti. Kaikki hoito-ohjelman aikana kerätty tieto käsitellään luottamuksellisena eikä hoito-ohjelmaan osallistuvan henkilöllisyys käy ilmi tehtävissä yhteenvedoissa eikä raporteissa. Suomen Hematologista Rekisteriä, johon tiedot kootaan, säilytetään tietosuojalainsäädännön edellyttämällä tavalla ja sen käyttö on hyväksytty Teitä hoitavassa sairaalassa.